Содержание
- Определение привычного невынашивания
- Классификация причин невынашивания
- Генетические причины потери беременности
- Негенетические причины невынашивания беременности
- Диагностика после потери беременности
- Генетическое исследование абортивного материала
- Что дают результаты
- Прегравидарная терапия: коррекция выявленных нарушений перед следующей беременностью
- Как выбрать исследование при потере беременности
- Сравнительная таблица диагностических возможностей, ограничений и показаний для выбора анализа абортивного материала:
Самопроизвольное прерывание беременности остаётся одной из наиболее частых проблем в репродуктивной медицине. По данным крупных популяционных исследований, от 10 до 15% клинически подтверждённых беременностей заканчиваются потерей, а с учётом доклинических (биохимических) беременностей частота потерь может достигать 40–50%. Эти цифры означают, что значительная часть зачатий прерывается на самых ранних этапах, нередко ещё до того, как женщина осознаёт факт беременности.
Подавляющее большинство спорадических потерь первого триместра обусловлено хромосомными аномалиями эмбриона и представляет собой механизм естественного отбора, элиминирующий нежизнеспособные зародыши. Вероятность благополучного исхода следующей беременности после единственной потери превышает 80–85%. Однако с каждой последующей потерей эта вероятность снижается, а спектр возможных причин расширяется за счёт систематически действующих материнских факторов.
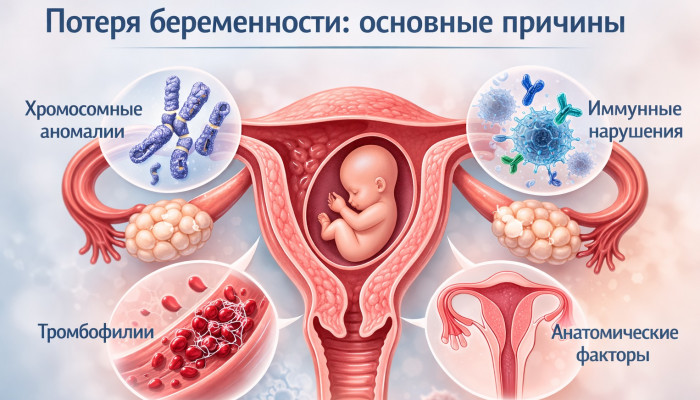
Невынашивание беременности — проблема мультифакториальная. Причина может быть генетической (аномалии хромосомного набора или мутации отдельных генов у эмбриона), анатомической (пороки развития или приобретённые изменения матки), эндокринной (гормональный дисбаланс, нарушающий условия для имплантации и развития), иммунологической (патологическая активация иммунной системы матери против тканей плода), тромбофилической (склонность к тромбообразованию в сосудах плаценты), инфекционной (хроническое или острое воспаление эндометрия и плодных оболочек). В значительной части случаев причина остаётся неустановленной, и такие потери классифицируются как идиопатические. Нередко у одной пациентки обнаруживается сочетание нескольких факторов, действующих одновременно. Именно эта мультифакториальность определяет необходимость комплексного подхода к обследованию.
После потери беременности у врача и пациентки есть очень короткое окно для решения, какой материал и на какое исследование направить. Практически это главный вопрос первых часов: сохранять свежий материал для генетического анализа или материал уже будет направлен на стандартную гистологическую обработку с фиксацией и заливкой в парафин. Именно этот выбор определяет, будут ли доступны методы максимального генетического охвата, такие как кариотипирование и хромосомный микроматричный анализ (ХМА), или диагностический маршрут будет строиться уже вокруг исследований из парафинового блока.
Определение привычного невынашивания
В клинической практике принципиально разграничение спорадической потери и привычного невынашивания беременности (recurrent pregnancy loss, RPL). Спорадическая потеря — однократный эпизод самопроизвольного прерывания, чаще всего обусловленный случайной хромосомной аномалией эмбриона. Традиционно привычное невынашивание определялось как три и более последовательные потери беременности до 22 недель гестации. Однако современные рекомендации ESHRE и ASRM рассматривают клиническую целесообразность обследования уже после двух последовательных потерь, поскольку вероятность повторения в этой группе существенно возрастает.
Это разграничение имеет прямое практическое значение. От того, к какой категории относится конкретная клиническая ситуация, зависит объём обследования, выбор метода исследования абортивного материала и стратегия подготовки к следующей беременности. Тактика после первой потери у молодой женщины и тактика после третьей потери у пациентки старше 35 лет — это принципиально разные диагностические алгоритмы.
Классификация причин невынашивания
Систематизация причин невынашивания позволяет выстроить логику обследования и не упустить ни одного значимого фактора. Все причины подразделяются на две большие группы: генетические (связанные с хромосомными или генными нарушениями у эмбриона) и негенетические (связанные с состоянием организма матери). Генетические причины включают хромосомные аномалии (анеуплоидии, полиплоидии, структурные перестройки) и моногенные заболевания. Негенетические объединяют анатомические, эндокринные, иммунологические, тромбофилические и инфекционные факторы. Отдельную категорию составляет идиопатическое невынашивание, при котором установить причину не удаётся даже после полного обследования.
Исследование абортивного материала позволяет оценить первую группу причин (генетические), а при комплексном подходе (генетика + гистология) — получить косвенную, но клинически значимую информацию о ряде негенетических факторов: тромбофилиях, воспалении, нарушениях иммунной толерантности. Остальные негенетические причины диагностируются при обследовании самой пациентки.
Генетические причины потери беременности
Анеуплоидии. Хромосомные аномалии эмбриона являются ведущей причиной ранних репродуктивных потерь. В зависимости от метода анализа (классическое кариотипирование, сравнительная геномная гибридизация, секвенирование нового поколения) хромосомные аномалии выявляются в 50–70% случаев самопроизвольного прерывания беременности в первом триместре. К наиболее частому типу нарушений относят анеуплоидии, то есть изменение числа отдельных хромосом. Трисомии (наличие дополнительной третьей копии хромосомы) составляют около 60% всех хромосомных аномалий в абортивном материале. Чаще всего обнаруживаются трисомии по 16, 22, 21, 15 и 13 хромосомам. Моносомия X (кариотип 45,X) – вторая по частоте находка, на долю которой приходится до 20% хромосомно-аномальных потерь.
Большинство анеуплоидий возникает в результате нерасхождения хромосом в процессе созревания яйцеклетки (мейотическое нерасхождение) и представляет собой случайное событие, не связанное с наследственной предрасположенностью. Однако вероятность таких ошибок существенно возрастает с возрастом женщины. Считается, что ключевую роль играет возрастное нарушение системы когезии хромосом в ооцитах (ослабление белковых комплексов, удерживающих хроматиды вместе до момента их расхождения при делении), что приводит к преждевременному разделению хромосом и неправильному их распределению между дочерними клетками. Если у женщин моложе 30 лет доля хромосомно-аномальных эмбрионов составляет около 30–35%, то к 40 годам она превышает 60%, а после 42 лет может достигать 80%. Именно этот феномен объясняет резкое возрастание частоты выкидышей и замерших беременностей в позднем репродуктивном возрасте и служит основанием для снижения порога обследования у пациенток старше 35 лет.
Помимо полных анеуплоидий, в абортивном материале нередко выявляется хромосомный мозаицизм, при котором в тканях эмбриона одновременно присутствуют клеточные линии с различным числом хромосом. Мозаицизм возникает вследствие ошибок митотического деления на ранних стадиях эмбриогенеза (то есть уже после оплодотворения, при делении клеток зародыша) и обнаруживается приблизительно в 10–15% случаев. Клиническое значение мозаицизма зависит от доли аномальных клеток и типа поражённой ткани: при высокой доле аномальных клеток мозаицизм может быть непосредственной причиной потери, тогда как низкий уровень мозаицизма иногда совместим с развитием беременности, но ассоциирован с повышенным риском осложнений.
Полиплоидии. При данной патологии происходит кратное увеличение всего хромосомного набора, полиплоидии составляют 15–20% хромосомных аномалий при ранних потерях. Основные варианты: триплоидия (69 хромосом, три полных набора) и тетраплоидия (92 хромосомы, четыре набора). Оба состояния, как правило, несовместимы с жизнью. Триплоидия может возникать несколькими путями: при одновременном оплодотворении яйцеклетки двумя сперматозоидами (диспермия), при оплодотворении диплоидным сперматозоидом, не прошедшим нормальное редукционное деление, или при созревании диплоидной яйцеклетки вследствие нарушения мейоза. Механизм возникновения имеет прямое клиническое значение: триплоидия отцовского происхождения (дополнительный набор от отца) ассоциирована с частичным пузырным заносом и риском гестационной трофобластической болезни, тогда как триплоидия материнского происхождения обычно приводит к ранней гибели эмбриона без риска трофобластической патологии. Тетраплоидия встречается значительно реже и приводит к прерыванию на самых ранних сроках.
Структурные перестройки хромосом. Транслокации, инверсии, делеции и дупликации обнаруживаются в абортивном материале реже, чем анеуплоидии и полиплоидии, однако имеют принципиально иное клиническое значение. Несбалансированная структурная перестройка у эмбриона может быть следствием носительства сбалансированной транслокации или инверсии у одного из родителей. Носитель клинически здоров — общее количество генетического материала у него не изменено, — однако при формировании половых клеток с высокой вероятностью образуются несбалансированные варианты, содержащие избыток или дефицит хромосомного материала. Это приводит к повторным потерям беременности или рождению ребёнка с хромосомной патологией. По данным цитогенетических исследований, приблизительно в 3–5% пар с привычным невынашиванием один из партнёров является носителем сбалансированной перестройки (чаще всего робертсоновской или реципрокной транслокации). Выявление такой перестройки кардинально меняет тактику: паре показано медико-генетическое консультирование и преимплантационное генетическое тестирование при планировании следующей беременности.
Моногенные причины. Отдельную и пока недостаточно изученную категорию генетических причин невынашивания составляют моногенные нарушения — мутации в отдельных генах, не затрагивающие структуру или число хромосом. Стандартные методы исследования абортивного материала (кариотипирование, хромосомный микроматричный анализ, фрагментный анализ) не выявляют моногенные мутации, поскольку работают на уровне хромосом, а не отдельных генов. Тем не менее ряд исследований с применением экзомного секвенирования абортивного материала показывает, что патогенные моногенные варианты могут обнаруживаться в 10–20% случаев привычного невынашивания с нормальным хромосомным набором эмбриона. Наиболее часто выявляются мутации в генах, контролирующих раннее эмбриональное развитие, формирование сердечно-сосудистой системы и скелета. Клиническое применение экзомного секвенирования абортивного материала пока остаётся в области научных исследований и не входит в стандартные диагностические алгоритмы, однако при необъяснимом привычном невынашивании с повторно нормальным хромосомным набором эмбриона этот подход может обсуждаться на консультации генетика.
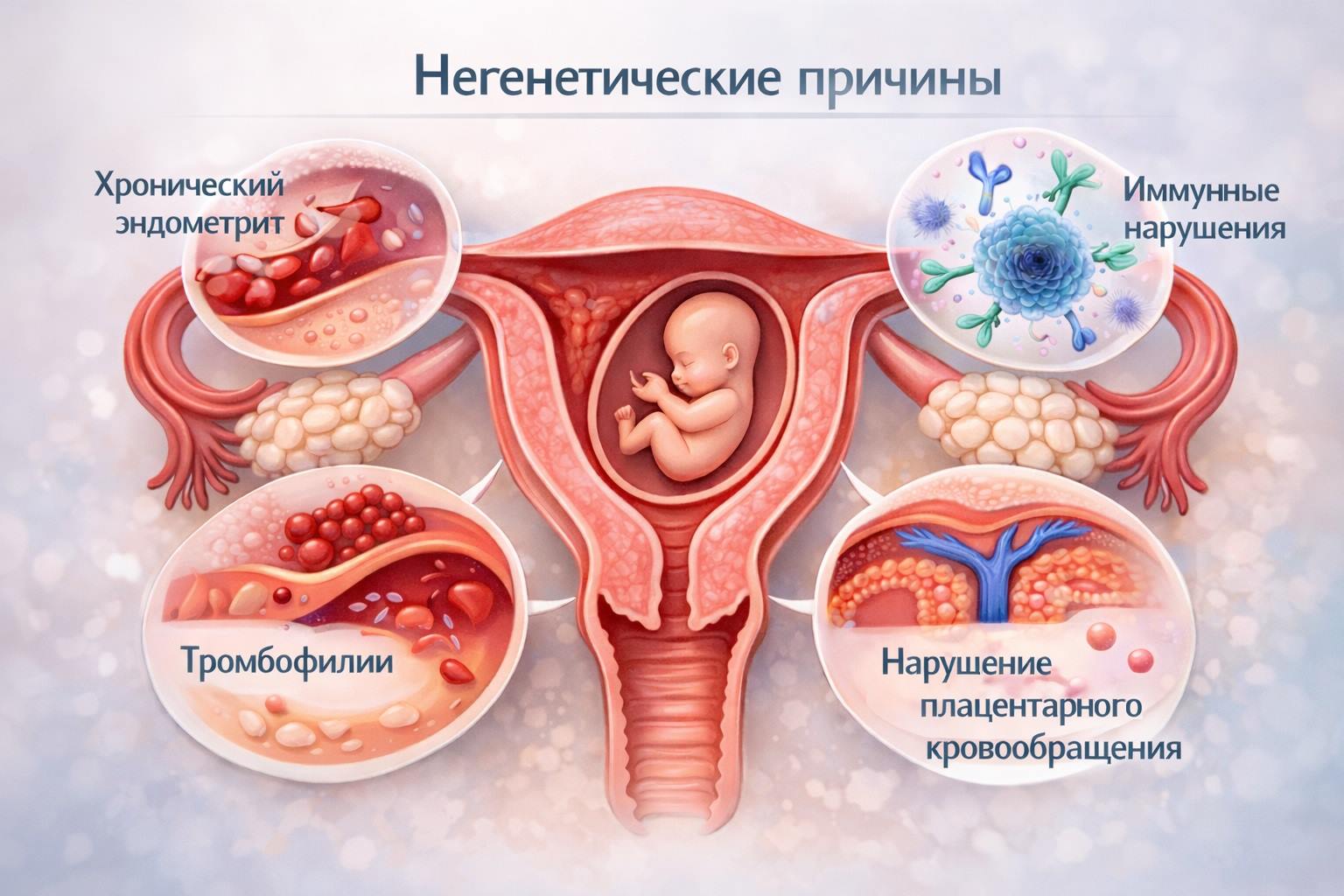
Негенетические причины невынашивания беременности
Если хромосомный набор эмбриона оказывается нормальным, причину потери следует искать в организме матери. Негенетические факторы невынашивания многообразны, и нередко у одной пациентки обнаруживается сочетание нескольких из них.
Анатомические факторы. Врождённые аномалии строения матки (двурогая, седловидная, однорогая матка, внутриматочная перегородка) нарушают условия для имплантации и развития плодного яйца. Внутриматочная перегородка считается наиболее клинически значимой аномалией: её ткань бедно васкуляризована и не способна обеспечить полноценного питания эмбриона. Приобретённые анатомические нарушения — субмукозная миома матки, внутриматочные синехии (сращения после воспалительных процессов или внутриматочных вмешательств), полипы эндометрия — также ассоциированы с повторными потерями. Диагностика проводится с помощью ультразвукового исследования, гистероскопии и магнитно-резонансной томографии.
Эндокринные нарушения. Недостаточность лютеиновой фазы (дефицит прогестерона во второй фазе менструального цикла) приводит к неполноценной децидуальной трансформации эндометрия — процессу, необходимому для принятия и удержания эмбриона. Синдром поликистозных яичников (СПКЯ) ассоциирован с повышенным риском невынашивания через несколько механизмов: гиперандрогению, инсулинорезистентность, нарушение качества ооцитов. Заболевания щитовидной железы (гипотиреоз, аутоиммунный тиреоидит с повышенным уровнем антител к тиреопероксидазе) являются доказанным фактором риска потери беременности, поскольку тиреоидные гормоны играют ключевую роль в имплантации и раннем развитии эмбриона. Некомпенсированный сахарный диабет и гиперпролактинемия также входят в перечень эндокринных причин.
Иммунологические нарушения. Антифосфолипидный синдром (АФС) — наиболее изученная и клинически значимая иммунологическая причина привычного невынашивания. АФС характеризуется выработкой антител к фосфолипидам клеточных мембран (антикардиолипиновые антитела, антитела к бета-2-гликопротеину I, волчаночный антикоагулянт), что приводит к тромбозам мелких сосудов плаценты и нарушению маточно-плацентарного кровотока. Диагноз устанавливается при сочетании клинических критериев с лабораторным подтверждением циркуляции антифосфолипидных антител в двух исследованиях с интервалом не менее 12 недель. Терапия (низкомолекулярные гепарины и низкие дозы ацетилсалициловой кислоты) существенно улучшает прогноз. Помимо АФС, обсуждается роль аллоиммунных механизмов — нарушения иммунологической толерантности между организмом матери и генетически чужеродным плодом. Гистологическим проявлением этих процессов могут быть воспаление ворсин неустановленной этиологии (VUE) и хронический гистиоцитарный интервиллозит, выявляемые при морфологическом исследовании абортивного материала.
Тромбофилии. Наследственные нарушения в системе гемостаза — мутация фактора V Лейден, мутация гена протромбина (G20210A), дефицит протеина С, протеина S, антитромбина III — повышают склонность к тромбообразованию в сосудах плаценты. Морфологическим отражением этих нарушений являются инфаркты плацентарной ткани, тромбозы межворсинчатого пространства, недостаточное ремоделирование спиральных артерий — картина, которую патоморфолог описывает как материнскую сосудистую мальперфузию. Выявление этих морфологических признаков при гистологическом исследовании абортивного материала служит прямым основанием для прицельного обследования пациентки на тромбофилии.
Инфекционные факторы. Хронический эндометрит — персистирующее воспаление слизистой оболочки матки, подтверждаемое наличием плазматических клеток в строме эндометрия, — рассматривается как самостоятельная и поддающаяся лечению причина привычного невынашивания и неудач имплантации при ЭКО. Острые инфекции (хориоамнионит, вызванный восходящей бактериальной флорой) чаще становятся причиной потерь во втором триместре. Роль TORCH-инфекций (токсоплазмоз, краснуха, цитомегаловирус, герпес) как систематически действующего фактора привычного невынашивания остаётся дискуссионной: эти инфекции могут вызывать гибель эмбриона, но обычно не рецидивируют из беременности в беременность.
Идиопатическое невынашивание. Несмотря на полное обследование, в 25–50% случаев привычного невынашивания установить причину не удаётся. Важно подчеркнуть, что прогноз при идиопатическом RPL в целом благоприятный: вероятность успешной беременности при последующих попытках составляет 60–75% даже без специфической терапии. Отсутствие установленной причины не означает отсутствие причины как таковой — оно указывает на ограничения современных диагностических возможностей, включая вероятную роль пока не идентифицированных моногенных, эпигенетических и иммунологических механизмов.
Диагностика после потери беременности
Тактика обследования после потери беременности определяется количеством предшествующих потерь, возрастом пациентки и клиническим контекстом.
Первая потеря. У молодой женщины (до 35 лет) после единственной потери объём обследования может быть минимальным. Базовый генетический скрининг абортивного материала подтверждает или исключает хромосомную причину, а гистологическое исследование оценивает состояние тканей. Комплексное исследование абортивного материала, объединяющее оба компонента, оптимально решает обе задачи из одного парафинового блока. Расширенное генетическое тестирование, поиск тромбофилий, развёрнутое иммунологическое обследование на этом этапе, как правило, избыточны.
Две потери. После двух последовательных потерь, особенно у женщин старше 35 лет, вероятность систематически действующего фактора возрастает. На этом этапе целесообразно расширить генетическое исследование абортивного материала (добавить панель микроделеционных синдромов), провести кариотипирование обоих партнёров, исследовать антифосфолипидные антитела и основные показатели гемостаза.
Три и более потери (привычное невынашивание). Показано полное обследование: методы с максимальным диагностическим охватом для исследования абортивного материала (хромосомный микроматричный анализ при наличии свежего материала или расширенное комплексное генетическое и гистологическое исследование при парафиновом блоке), кариотипирование обоих партнёров, развёрнутое обследование на тромбофилии и АФС, оценка анатомии матки (гистероскопия, МРТ), эндокринный профиль (тиреоидная функция, прогестерон, инсулинорезистентность), при необходимости — иммунологическое обследование.
Возраст как модификатор тактики. У пациенток старше 35 лет порог для расширенного обследования снижается: углублённая диагностика обоснована уже после двух потерь. У женщин старше 40 лет расширенное обследование может быть рекомендовано уже после первой потери при наличии настораживающих признаков — аномальная ультразвуковая картина, подозрение на пузырный занос, анамнез неудачных циклов ЭКО.
Что даёт гистология в связке с генетикой. Комплексные исследования, объединяющие хромосомный анализ и гистологию, информативнее суммы двух отдельных анализов. Хромосомная аномалия плода объясняет причину текущей потери, но гистологическая картина может одновременно выявить сопутствующую материнскую патологию — признаки тромбофилии, хронический эндометрит, нарушение трофобластической инвазии, воспаление ворсин. Эти находки не отменяют генетическую причину данной потери, но указывают на факторы, способные осложнить следующую беременность. Верно и обратное: при нормальном хромосомном наборе эмбриона именно гистология становится единственным источником информации о причине прерывания и направляет дальнейший диагностический поиск.
Генетическое исследование абортивного материала
Исследование абортивного материала — важный компонент диагностики причин потери беременности. Существует несколько методов, различающихся по технологии, диагностическому охвату и требованиям к биоматериалу.
Момент выбора: свежий материал или парафиновый блок. Принципиальное практическое разделение всех методов проходит по типу биоматериала. Кариотипирование и хромосомный микроматричный анализ (ХМА) требуют свежей ткани, помещённой в стерильный контейнер с физиологическим раствором непосредственно после получения материала — при хирургическом выскабливании, вакуум-аспирации или самопроизвольном выкидыше в условиях стационара. Решение о проведении этих анализов должно быть принято заблаговременно. Если момент упущен и материал направлен на стандартную гистологическую обработку (фиксация формалином, заливка в парафин), кариотипирование и ХМА выполнить уже невозможно.
Для методов, работающих с парафиновыми блоками (хромосомный скрининг, расширенное хромосомное исследование, комплексные анализы с гистологией), момент принятия решения не критичен. Парафиновый блок хранится в патоморфологической лаборатории и может быть использован для генетического анализа спустя недели и месяцы после потери. Это существенное преимущество для ситуаций, когда решение об обследовании принимается ретроспективно — на приёме у гинеколога или репродуктолога уже после выписки.
Доступные методы. Хромосомный скрининг [Исследование хромосом в абортивном материале, скрининг ] выполняется методом диагностического фрагментного анализа из парафинового блока и выявляет анеуплоидии всех хромосом, субтеломерные делеции и дупликации, определяет наличие Y-хромосомы. Это базовый анализ для первичной оценки хромосомных причин. Расширенное хромосомное исследование [Исследование хромосом в абортивном материале, расширенное ] использует тот же метод, но дополнительно включает панель из 30 микроделеционных и микродупликационных синдромов. Кариотипирование абортного материала [Хромосомный анализ абортного материала, (кариотип плода) ] — классический цитогенетический метод (культивирование клеток, GTG-бэндинг), единственный способ выявления сбалансированных перестроек; требует свежего материала, риск неудачи культивирования 5–40%. Хромосомный микроматричный анализ [Хромосомный микроматричный анализ абортного материала ] выполняется на SNP-микроматрицах из свежего материала и обеспечивает максимально широкий молекулярный охват: анеуплоидии, триплоидия с определением родительского происхождения, однородительская дисомия, субмикроскопические делеции и дупликации по всему геному, надёжное выявление контаминации материнскими клетками. Комплексное генетическое и гистологическое исследование выпускается в двух вариантах — скрининговом [Комплексное генетическое и гистологическое исследование абортивного материала, скрининг ] и расширенном [Комплексное генетическое и гистологическое исследование абортивного материала, расширенное ], объединяя соответствующий генетический анализ с полноценным гистологическим исследованием из одного парафинового блока.
Проблема результата 46,XX. Результат, требующий особой осторожности при интерпретации, — нормальный женский хромосомный набор (46,XX). Он может принадлежать как эмбриону женского пола, так и материнским клеткам, попавшим в образец при смешивании тканей. Ни один метод, работающий с парафиновым блоком, не способен достоверно разграничить клетки эмбриона и матери при женском поле плода. ХМА на SNP-платформе решает эту проблему за счёт генотипирования: сравнение аллельных профилей позволяет определить происхождение клеток. При получении результата 46,XX на парафиновом блоке в ситуации привычного невынашивания целесообразно заблаговременно обсудить с врачом сбор свежего материала при следующей потере для проведения ХМА.

Ограничения всех методов. Все шесть вариантов исследования работают на уровне хромосом и не выявляют моногенные мутации, эпигенетические нарушения (за исключением ОРД, выявляемой ХМА), анатомические аномалии матки, эндокринные нарушения. Гистологический компонент комплексных исследований может обнаружить морфологические последствия тромбофилий, воспаления, иммунных нарушений, но не идентифицирует конкретный возбудитель инфекции и не заменяет лабораторное обследование крови на тромбофилии и АФС. Подробное сравнение диагностических возможностей всех шести анализов приведено в сравнительной таблице в конце статьи.
Что дают результаты
Результаты исследования абортивного материала формируют доказательную базу для целенаправленной подготовки к следующей беременности, позволяя перейти от эмпирического лечения к обоснованной стратегии.
При выявлении случайной анеуплоидии прогноз, как правило, благоприятный. Специфической подготовки не требуется, однако у женщин старшего репродуктивного возраста может быть рекомендовано преимплантационное генетическое тестирование на анеуплоидии (ПГТ-А) в цикле ЭКО для отбора эмбрионов с нормальным хромосомным набором.
Обнаружение несбалансированной структурной перестройки у эмбриона требует кариотипирования обоих партнёров. При выявлении сбалансированной транслокации или инверсии у одного из родителей показано преимплантационное генетическое тестирование на структурные перестройки (ПГТ-СП), позволяющее отобрать эмбрионы с нормальным или сбалансированным набором.
Триплоидия отцовского происхождения (частичный пузырный занос) требует мониторинга уровня хорионического гонадотропина после эвакуации плодного яйца для исключения трофобластической неоплазии. Планирование следующей беременности рекомендуется после нормализации показателя и завершения периода наблюдения.
Гистологические находки формируют самостоятельный блок рекомендаций. Признаки материнской сосудистой мальперфузии служат основанием для обследования на тромбофилии и АФС с последующей антикоагулянтной терапией при следующей беременности. Хронический эндометрит требует антибактериальной терапии с контрольной биопсией эндометрия до наступления беременности. Воспаление ворсин неустановленной этиологии (VUE) с риском рецидива до 30% может потребовать иммуномодулирующей терапии, хотя стандартизированные протоколы лечения этого состояния пока не разработаны. Признаки недостаточной трофобластической инвазии и неполноценной децидуализации эндометрия указывают на необходимость гормонального обследования и коррекции прогестероновой поддержки.
Когда ни генетический анализ, ни гистология не выявляют значимых изменений, необходимо расширить диагностический поиск: оценить анатомию матки, исследовать эндокринный профиль, провести развёрнутое иммунологическое обследование. Отсутствие находок при исследовании абортивного материала означает не отсутствие причины, а необходимость искать её другими методами.
Планирование следующей беременности после потери — всегда совместная работа пациентки с акушером-гинекологом и, при необходимости, генетиком, гематологом, эндокринологом, иммунологом. Результаты исследования абортивного материала не дают готовых рецептов, но создают фундамент для осознанных клинических решений и позволяют каждой паре двигаться к цели по индивидуальному, научно обоснованному маршруту.
Прегравидарная терапия: коррекция выявленных нарушений перед следующей беременностью
Результаты обследования после потери беременности приобретают практическую ценность лишь тогда, когда трансформируются в конкретную терапевтическую стратегию. Прегравидарная подготовка — период целенаправленного лечения и коррекции выявленных нарушений до наступления следующей беременности — является критическим этапом, определяющим её исход. Каждый выявленный фактор требует собственного терапевтического подхода, и ниже рассмотрены основные направления коррекции.
Антикоагулянтная терапия при антифосфолипидном синдроме и тромбофилиях. Антифосфолипидный синдром — единственная иммунологическая причина привычного невынашивания, для которой разработана терапия с доказанной эффективностью. Стандартом лечения является комбинация низкомолекулярного гепарина (НМГ) и низких доз ацетилсалициловой кислоты (75–100 мг в сутки). Ацетилсалициловая кислота назначается с момента планирования беременности или с положительного теста, низкомолекулярный гепарин в профилактических дозах (эноксапарин 40 мг в сутки или далтепарин 5000 МЕ в сутки подкожно) — с подтверждения маточной беременности. Терапия НМГ продолжается на протяжении всей беременности и, как правило, в течение 6 недель после родоразрешения, поскольку послеродовый период сопряжён с повышенным тромботическим риском. Мониторинг включает регулярный контроль уровня тромбоцитов (для исключения гепарин-индуцированной тромбоцитопении), показателей коагулограммы и клиническое наблюдение за состоянием пациентки. По данным рандомизированных исследований, комбинированная терапия повышает частоту живорождения при АФС с 40–50% без лечения до 70–80%.
При наследственных тромбофилиях (мутация фактора V Лейден, мутация гена протромбина, дефицит естественных антикоагулянтов) тактика определяется индивидуально. Гомозиготные формы мутаций и комбинированные тромбофилии, как правило, требуют профилактических доз НМГ на протяжении беременности. При гетерозиготных формах решение о назначении антикоагулянтной терапии принимается с учётом акушерского анамнеза, наличия дополнительных факторов риска и данных гистологического исследования: морфологические признаки материнской сосудистой мальперфузии (инфаркты, тромбозы, децидуальная артериопатия) при предшествующей потере являются дополнительным аргументом в пользу антикоагулянтной профилактики.
Лечение хронического эндометрита. Хронический эндометрит — одна из немногих причин привычного невынашивания, поддающихся полному излечению. Терапия основана на назначении антибактериальных препаратов широкого спектра, поскольку в большинстве случаев хронический эндометрит ассоциирован с полимикробной флорой. Наиболее распространённые схемы включают комбинацию доксициклина (100 мг дважды в сутки в течение 14 дней) с метронидазолом или фторхинолоном. При выявлении специфического возбудителя (Ureaplasma, Mycoplasma, Chlamydia) терапия корректируется по результатам антибиотикочувствительности.
Критически важным этапом является контроль излеченности. Через 2–4 недели после завершения курса антибиотикотерапии выполняется контрольная пайпель-биопсия эндометрия с иммуногистохимическим определением маркера плазматических клеток (CD138). Исчезновение плазмоцитов из стромы эндометрия подтверждает элиминацию хронического воспаления. При сохранении признаков эндометрита проводится повторный курс со сменой антибактериальной схемы. Планирование беременности рекомендуется только после документированного излечения.
В последние годы всё больше внимания уделяется восстановлению микробиома эндометрия после антибиотикотерапии. Появляются данные о том, что преобладание лактобацилл в полости матки (так называемый Lactobacillus-доминантный эндометриальный микробиом) ассоциировано с лучшими исходами имплантации и беременности. В связи с этим ряд клиницистов рекомендует применение вагинальных и пероральных пробиотиков, содержащих штаммы Lactobacillus, после завершения антибактериальной терапии. Доказательная база по эффективности этого подхода пока формируется, однако восстановление нормальной микробной среды представляется патогенетически обоснованным.
Эндокринная коррекция. Прогестероновая поддержка является одним из наиболее часто назначаемых компонентов прегравидарной подготовки и ведения ранних сроков беременности при привычном невынашивании. Микронизированный прогестерон (200–400 мг в сутки вагинально) или дидрогестерон (20–30 мг в сутки перорально) назначается с момента овуляции или положительного теста на беременность и продолжается, как правило, до 12–16 недель гестации. Крупное многоцентровое исследование PROMISE и последующий метаанализ показали, что прогестероновая поддержка наиболее эффективна именно в группе женщин с привычным невынашиванием (три и более потери), где она достоверно увеличивает частоту живорождения. При недостаточности лютеиновой фазы, подтверждённой гистологически (неполноценная децидуализация эндометрия) или лабораторно (низкий уровень прогестерона в середине лютеиновой фазы), назначение прогестерона особенно обосновано.
Коррекция тиреоидной функции обязательна при выявлении гипотиреоза или субклинического гипотиреоза. Целевой уровень тиреотропного гормона (ТТГ) на этапе планирования и в первом триместре беременности составляет менее 2,5 мМЕ/л. Заместительная терапия левотироксином назначается под контролем ТТГ и свободного Т4. При аутоиммунном тиреоидите с повышенным уровнем антител к тиреопероксидазе (АТ-ТПО) даже при нормальном ТТГ ряд экспертов рекомендует профилактическое назначение левотироксина в малых дозах, поскольку носительство АТ-ТПО само по себе ассоциировано с повышенным риском невынашивания. Механизм этой связи до конца не ясен и, вероятно, включает как субклиническую тиреоидную недостаточность, так и общую иммунологическую дисрегуляцию.
При синдроме поликистозных яичников коррекция направлена на несколько звеньев патогенеза. Метформин (1500–2000 мг в сутки) применяется для снижения инсулинорезистентности, которая рассматривается как один из механизмов повышенного риска невынашивания при СПКЯ. Данные ряда исследований свидетельствуют о том, что продолжение приёма метформина в первом триместре может снижать частоту выкидышей у пациенток с СПКЯ, хотя этот вопрос остаётся предметом дискуссии. Нормализация массы тела, коррекция гиперандрогении, достижение регулярной овуляции являются обязательными компонентами подготовки. При некомпенсированном сахарном диабете планирование беременности допускается только после достижения целевых показателей гликированного гемоглобина (HbA1c менее 6,5%).
Иммуномодулирующая терапия. Иммунологические поражения плаценты — воспаление ворсин неустановленной этиологии (VUE), хронический гистиоцитарный интервиллозит, массивное периворсинчатое отложение фибрина — ассоциированы с высоким риском повторных потерь, однако стандартизированные протоколы их лечения до настоящего времени не разработаны. Терапия носит эмпирический характер и основана на патогенетическом обосновании: все перечисленные состояния рассматриваются как проявления нарушения иммунологической толерантности между организмом матери и плода.
При рецидивирующем VUE и хроническом гистиоцитарном интервиллозите применяются глюкокортикостероиды (преднизолон 10–20 мг в сутки с первого триместра с постепенным снижением дозы), в ряде случаев в комбинации с низкими дозами ацетилсалициловой кислоты и НМГ. При тяжёлых рецидивирующих формах интервиллозита, приводящих к повторным потерям во втором и третьем триместрах, описано применение внутривенного иммуноглобулина (ВВИГ) в дозах 400–1000 мг/кг ежемесячно. Данные об эффективности ВВИГ при этих состояниях получены преимущественно из серий случаев и небольших когортных исследований, а не из рандомизированных контролируемых испытаний, что ограничивает уровень доказательности. Тем не менее при отсутствии альтернативных терапевтических опций и высоком риске рецидива иммуномодулирующая терапия рассматривается как клинически обоснованный подход.
При массивном периворсинчатом отложении фибрина описаны схемы с ранним назначением гепарина, ацетилсалициловой кислоты и преднизолона, начиная с прегравидарного периода или первых недель беременности. Эффективность этих схем неоднородна: у части пациенток удаётся предотвратить рецидив, тогда как в других случаях поражение рецидивирует несмотря на терапию. Каждый случай требует индивидуального обсуждения в мультидисциплинарной команде (акушер-гинеколог, иммунолог, гематолог, патоморфолог) с обязательным информированием пациентки о текущем уровне доказательности предлагаемого лечения.
Важно подчеркнуть, что диагностика иммунологических поражений плаценты возможна только при гистологическом исследовании абортивного материала. Без морфологической верификации назначение иммуномодулирующей терапии лишено обоснования. Это ещё одна причина, по которой комплексное исследование абортивного материала (генетика + гистология) предпочтительнее изолированного генетического анализа: гистологический компонент может выявить именно те состояния, которые требуют специфического и нередко длительного лечения перед следующей беременностью.
Как выбрать исследование при потере беременности
Практически во все клинические рекомендации по привычному невынашиванию включено положение о том, что хромосомные аномалии плода являются причиной 50–70% ранних потерь беременности. Поэтому оптимальная тактика обследования начинается с ответа на ключевой вопрос: была ли потеря связана с генетическим фактором. Ниже приведён упрощённый алгоритм выбора исследования, который поможет врачу и пациентке сориентироваться в доступных вариантах.
Первая потеря беременности. В большинстве случаев достаточно базового генетического скрининга абортивного материала, который подтвердит или исключит хромосомную причину. При необходимости оценить и негенетические факторы (состояние эндометрия, ворсин хориона, наличие воспалительных или сосудистых нарушений) к генетическому скринингу добавляется морфологическая оценка тканей. Оптимальный выбор для этой ситуации — комплексное исследование абортивного материала, скрининг, объединяющее генетику и гистологию в одном анализе из парафинового блока. Для молодой женщины с первым эпизодом потери этого объёма, как правило, достаточно.
Повторные потери беременности (две и более). С каждой последующей потерей вероятность систематически действующего фактора возрастает. На этом этапе требуется расширенный генетический анализ, включающий панель микроделеционных и микродупликационных синдромов, а также желательна морфологическая оценка плацентарных тканей для выявления тромбофилических, воспалительных и иммунологических изменений. Оптимальный выбор — расширенное хромосомное исследование или комплексное генетическое и гистологическое исследование, расширенное. Параллельно рекомендуется кариотипирование обоих партнёров для исключения носительства сбалансированных перестроек.
Привычное невынашивание (три и более потерь). Необходимо исключить весь спектр генетических причин: структурные перестройки хромосом, полиплоидии, микроделеции, редкие геномные нарушения, однородительскую дисомию. Оптимальный выбор определяется типом доступного материала. Если свежий материал собран непосредственно после получения, наиболее информативны кариотипирование абортного материала (единственный метод, выявляющий сбалансированные перестройки) и хромосомный микроматричный анализ (максимально широкий молекулярный охват с определением родительского происхождения генома). При подозрении на пузырный занос предпочтителен ХМА. В идеале при привычном невынашивании целесообразно проведение обоих исследований параллельно, поскольку они дополняют друг друга: кариотипирование обнаруживает сбалансированные перестройки, недоступные для ХМА, а ХМА выявляет субмикроскопические нарушения и однородительскую дисомию, недоступные для кариотипирования.
Если материал уже прошёл патоморфологическую обработку. Ситуация, когда решение о генетическом исследовании принимается уже после фиксации и заливки материала в парафин, встречается часто. В этом случае кариотипирование и ХМА невозможны, однако архивный парафиновый блок позволяет выполнить хромосомный скрининг, расширенное хромосомное исследование или комплексный анализ с гистологией. Возможность ретроспективного генетического исследования — принципиальное преимущество методов, работающих с парафином: даже если при потере беременности свежий материал не был собран, генетическая диагностика остаётся доступной. При повторных потерях и привычном невынашивании рекомендуется заблаговременно обсудить с лечащим врачом сбор свежего материала в физиологический раствор при следующей потере, чтобы не ограничивать выбор метода.
Сравнительная таблица диагностических возможностей, ограничений и показаний для выбора анализа абортивного материала :
| Критерий | Исследование хромосом, скрининг | Исследование хромосом, расширенное | Кариотип плода | Хромосомный Микроматричный Анализ | Комплексное исследование, скрининг | Комплексное исследование, расширенное |
| Метод | Диагностический фрагментный анализ | Диагностический фрагментный анализ | Культивирование, GTG-бэндинг | SNP-микроматрица | Фрагментный анализ + гистология | Фрагментный анализ + гистология |
| Материал | Парафиновый блок | Парафиновый блок | Свежий материал в физрастворе | Свежий материал в физрастворе | Парафиновый блок со стёклами | Парафиновый блок со стёклами |
| Основные показания | Первая потеря беременности, когда достаточно базовой оценки хромосомных причин. Подходит, если вопрос о негенетических факторах пока не стоит | Повторные потери (два и более выкидыша); неудачи ЭКО; подозрение на микроделеционный синдром у плода по данным УЗИ; возраст матери старше 35 лет при повторной потере | Привычное невынашивание (три и более потери); подозрение на сбалансированную перестройку у одного из родителей (транслокация, инверсия); необходимость исключить полиплоидию | Привычное невынашивание; потребность в максимально широком молекулярном анализе; подозрение на пузырный занос или ОРД; случаи, когда кариотипирование неинформативно (неудача культивирования) | Первая потеря беременности, когда врач хочет одновременно оценить и хромосомные, и негенетические причины. Оптимальный выбор для молодой женщины с первым выкидышем — базовый генетический скрининг и полная морфологическая картина | Повторные потери; сочетание отягощённого анамнеза (тромбофилии, АФС, хронический эндометрит) с необходимостью расширенного генетического охвата; возраст матери старше 35 лет; неудачи ЭКО. Максимально полная картина причин потери из одного парафинового блока |
| Когда собирать материал | В любое время: используется архивный парафиновый блок после стандартной патоморфологической обработки | В любое время: используется архивный парафиновый блок после стандартной патоморфологической обработки | Сразу после получения: материал помещается в стерильный контейнер с физраствором и доставляется в лабораторию в кратчайшие сроки | Сразу после получения: материал помещается в стерильный контейнер с физраствором и доставляется в лабораторию в кратчайшие сроки | В любое время: используется архивный парафиновый блок после стандартной патоморфологической обработки | В любое время: используется архивный парафиновый блок после стандартной патоморфологической обработки |
| Необходимость живых клеток | Нет | Нет | Да | Нет | Нет | Нет |
| Анеуплоидии (трисомии, моносомии) всех хромосом | Да | Да | Да | Да | Да | Да |
| Субтеломерные делеции и дупликации | Да | Да | Крупные | Да | Да | Да |
| 30 микроделеционных/ микродупликационных синдромов | Нет | Да | Нет | Нет (выявляет другие микроделеции/микродупликации в пределах разрешения) | Нет | Да |
| Полиплоидии (триплоидия, тетраплоидия) | Нет | Нет | Да | Да (SNP-платформа) | Нет | Нет |
| Определение родительского происхождения триплоидии | Нет | Нет | Нет | Да | Нет | Нет |
| Сбалансированные перестройки (транслокации, инверсии) | Нет | Нет | Да | Нет | Нет | Нет |
| Мозаицизм | Нет | Нет | Да (при анализе ≥20 метафаз) | Ограниченно (порог 20–25%) | Нет | Нет |
| Однородительская дисомия (ОРД) | Нет | Нет | Нет | Да | Нет | Нет |
| Субмикроскопические делеции и дупликации по всему геному | Нет | Нет | Нет | Да | Нет | Нет |
| Определение пола плода (Y-хромосома) | Да | Да | Да | Да | Да | Да |
| Выявление контаминации материнскими клетками | Косвенно (по Y-хромосоме) | Косвенно (по Y-хромосоме) | Косвенно (по Y-хромосоме) | Да (SNP-генотипирование) | Косвенно (по Y-хромосоме) | Косвенно (по Y-хромосоме) |
| Гистологическое исследование (морфология тканей) | Нет | Нет | Нет | Нет | Да | Да |
| Выявление воспалительных изменений (хориоамнионит, децидуит, VUE) | Нет | Нет | Нет | Нет | Да | Да |
| Оценка маточно-плацентарного кровообращения (MVM, FVM) | Нет | Нет | Нет | Нет | Да | Да |
| Оценка трофобластической инвазии и гравидарных изменений эндометрия | Нет | Нет | Нет | Нет | Да | Да |
| Риск неинформативного результата | Минимальный | Минимальный | 5–40% (неудача культивирования) | Низкий | Минимальный | Минимальный |
| Когда собирать материал | В любое время: архивный парафиновый блок | В любое время: архивный парафиновый блок | Сразу после получения материала | Сразу после получения материала | В любое время: архивный парафиновый блок | В любое время: архивный парафиновый блок |
Информация, представленная в статье, носит справочный и образовательный характер. Окончательное решение о необходимости проведения генетического или морфологического исследования абортивного материала принимается лечащим врачом на основании клинической ситуации, анамнеза пациентки и результатов ранее выполненных обследований. Обсуждение диагностических возможностей исследования с врачом позволяет определить его целесообразность и выбрать наиболее информативный метод лабораторной диагностики.
