Фагоцитарная активность лейкоцитов.
20.08.2024
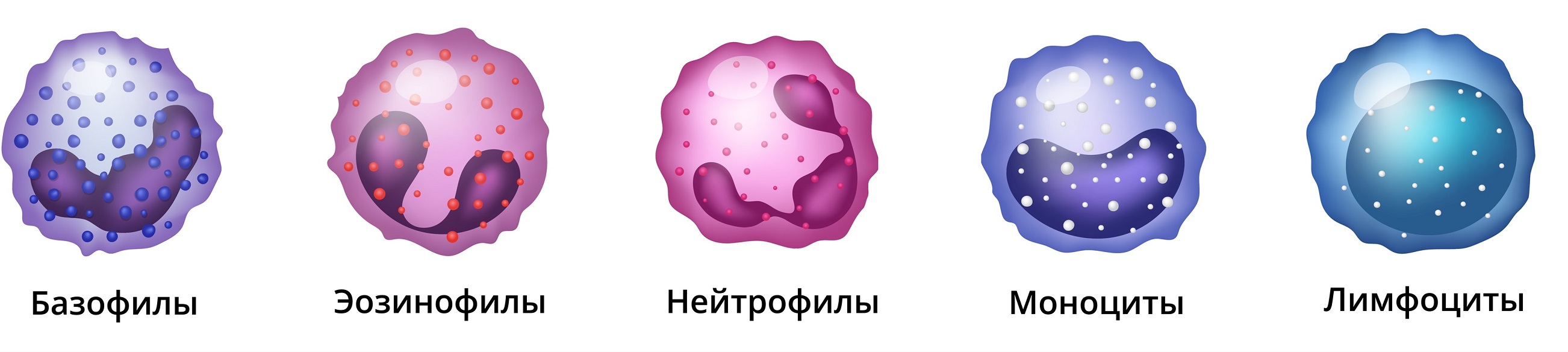
Фагоцитоз — это ключевой процесс, в котором клетки иммунной системы, такие как лейкоциты, поглощают и уничтожают чужеродные частицы, включая патогены и мёртвые клетки. Этот процесс играет важную роль в защите организма от инфекций и в регуляции воспалительных реакций. Лейкоциты, в частности нейтрофилы, моноциты и макрофаги, играют центральную роль в реализации фагоцитарной активности. Этот процесс является фундаментальной защитной реакцией организма, направленной на поддержание гомеостаза и предотвращение развития инфекционных заболеваний.
Фагоцитоз начинается с хемотаксиса, при котором лейкоциты мигрируют к очагу инфекции или воспаления в ответ на специфические химические сигналы. Эти сигналы могут включать цитокины, хемокины и продукты микробного метаболизма. По достижении места назначения лейкоциты распознают патогены или поврежденные клетки через рецепторы на своей поверхности, которые способны связываться с определенными молекулами-мишенями, такими как антитела, комплемент или компоненты клеточной стенки бактерий. Этот процесс распознавания известен как опсонизация и значительно повышает эффективность фагоцитоза.
После распознавания лейкоцит связывается с патогеном и происходит его поглощение путем инвагинации (впячивания внутрь) клеточной мембраны, при котором формируется внутриклеточный пузырек, называемый фагосомой. Внутрь фагосомы проникают гидролитические ферменты, уничтожающие поглощенный патогенный материал.
Фагоцитоз является не только механизмом уничтожения патогенов, но и важным процессом для презентации антигенов, что связывает врожденный и адаптивный (приобретенный) иммунитет. Определенные лейкоциты, такие как дендритные клетки и макрофаги, после фагоцитоза перерабатывают антигены и представляют их на своей поверхности в комплексе с молекулами главного комплекса гистосовместимости (MHC). Это позволяет Т-клеткам распознавать антигены и инициировать адаптивный иммунный ответ, что обеспечивает более специфическую и долговременную защиту организма.
Сдать общий анализ крови с лейкоформулой и СОЭ
Физиологическое значение фагоцитоза:
Удаление патогенов : При инфекции фагоциты мигрируют к очагу воспаления в ответ на хемотаксические сигналы, такие как продукты распада бактерий и цитокины, секретируемые повреждёнными клетками. Нейтрофилы первыми прибывают на место инфекции и начинают процесс фагоцитоза, поглощая и уничтожая бактерии. Макрофаги, которые приходят позже, продолжают этот процесс, дополнительно выделяя цитокины, которые усиливают воспалительный ответ.
Регуляция воспаления : Фагоциты не только уничтожают патогены, но и регулируют воспалительную реакцию. Макрофаги, например, выделяют провоспалительные цитокины, такие как TNF-α и IL-1, которые усиливают воспаление, а также антивоспалительные медиаторы, которые способствуют его разрешению. Это балансирует воспалительный процесс, предотвращая его чрезмерное развитие, которое может повредить собственные ткани организма.
Удаление апоптотических клеток : Ежедневно в организме человека происходит запрограммированная клеточная смерть (апоптоз), в результате которой формируются клетки, подлежащие удалению. Фагоциты играют важную роль в удалении этих клеток, предотвращая развитие воспаления и аутоиммунных реакций. Удаление апоптотических клеток без инициирования воспалительной реакции известно как "тихий фагоцитоз", который поддерживает тканевой гомеостаз.
Презентация антигенов : Макрофаги и дендритные клетки, после фагоцитоза патогенов, представляют их антигены на своей поверхности для активации Т-клеток. Этот процесс является важным для запуска адаптивного иммунного ответа, обеспечивая долгосрочную защиту организма через создание иммунологической памяти.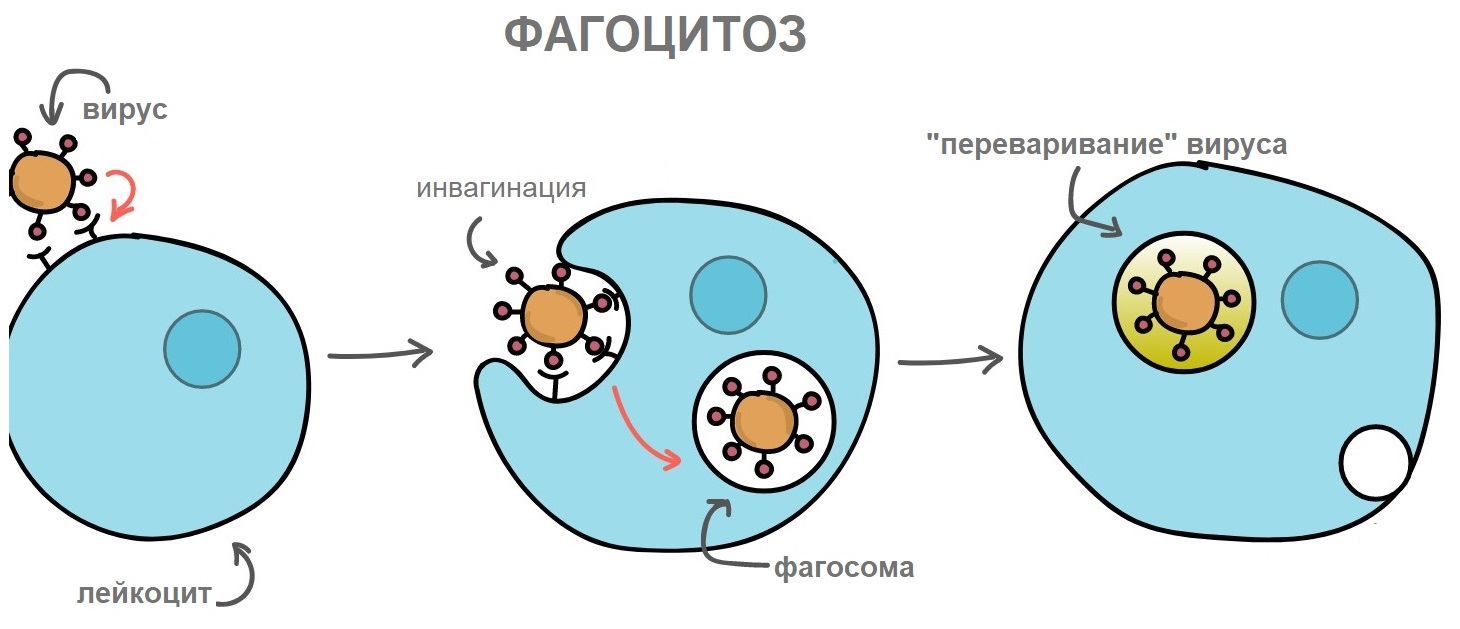
Нарушение фагоцитарной активности может привести к различным патологическим состояниям, включая хронические инфекции, аутоиммунные заболевания и иммунодефицитные состояния.
Наиболее значимые из них:
Хронические гранулематозные заболевания (ХГЗ): Это генетическое нарушение, при котором фагоциты не могут эффективно уничтожать поглощенные микроорганизмы из-за дефекта в NADPH-оксидазной системе, необходимой для генерации реактивных форм кислорода (РФО). В результате, организм не может адекватно бороться с некоторыми типами бактерий и грибков, что приводит к хроническим и рецидивирующим инфекциям, а также к формированию гранулём — скоплений активированных макрофагов и других клеток в попытке ограничить инфекцию.
Лейкоцитарная адгезионная недостаточность (ЛАН): Это редкое генетическое заболевание, при котором нарушена способность лейкоцитов мигрировать к очагу инфекции из-за дефекта в белках, участвующих в адгезии клеток к эндотелию сосудов. В результате, фагоциты не могут достичь места инфекции, что приводит к тяжёлым и рецидивирующим бактериальным инфекциям. Кроме того, пациенты с ЛАН часто страдают от плохого заживления ран и хронического воспаления.
Синдром Чедиака-Хигаши : Это редкое аутосомно-рецессивное заболевание, характеризующееся аномалиями в функции лизосом, которые приводят к нарушению фагоцитоза. Фагоциты пациентов с этим синдромом имеют крупные, но нефункциональные гранулы, что нарушает процесс уничтожения патогенов. Пациенты склонны к тяжёлым инфекциям, кровотечениям и имеют высокий риск развития лимфогистиоцитоза — состояния, при котором макрофаги чрезмерно активируются и начинают повреждать здоровые ткани.
Нейтропения : Снижение числа нейтрофилов (нейтропения) приводит к повышенной восприимчивости к инфекциям. Это состояние может быть врождённым (например, в случае циклической нейтропении) или приобретённым (например, вследствие химиотерапии или воздействия некоторых лекарств). При тяжёлой нейтропении организм становится крайне уязвимым к бактериальным и грибковым инфекциям, что требует немедленного медицинского вмешательства.
Аутоиммунные заболевания : В некоторых случаях нарушения в механизмах фагоцитоза могут способствовать развитию аутоиммунных заболеваний. Например, дефекты в "тихом фагоцитозе" могут привести к неполному удалению апоптотических клеток, что вызывает их распад и высвобождение внутриклеточных антигенов. Это может запустить аутоиммунный процесс, как в случае системной красной волчанки, где нарушение удаления апоптотических клеток играет важную роль в патогенезе.
Сепсис и синдром системного воспалительного ответа (ССВО) : В случае серьёзных инфекций фагоциты могут быть чрезмерно активированы, что приводит к массовому выбросу провоспалительных цитокинов и развитию сепсиса. ССВО — это системная реакция на инфекцию или повреждение тканей, которая может привести к множественным органным дисфункциям и шоку. При сепсисе нарушается баланс между провоспалительными и антивоспалительными процессами, что может привести к дисфункции фагоцитов и прогрессированию заболевания.
Сдать С-реактивный белок (CRP) в сыворотке крови
Для исследования фагоцитарной активности лейкоцитов рекомендуют несколько лабораторных тестов, которые помогают оценить способность клеток иммунной системы к поглощению и уничтожению патогенов, среди них:
Тест на фагоцитарную активность нейтрофилов : Этот тест предназначен для оценки способности нейтрофилов поглощать и уничтожать патогены или другие чужеродные частицы. В тесте обычно используют частички, которые имитируют патогены, напрмер латексные шарики или меченные бактерии (E. coli), которые инкубируются (помещаются в среду, имитирующую условия внутри организма) с нейтрофилами. После инкубации оценивают количество фагоцитированных частиц с помощью микроскопии или проточной цитометрии. Результаты дают информацию о проценте активных фагоцитов и их способности поглощать частицы.
HCT-тест (Hydrogen Peroxide Chemiluminescence Test) HCT-тест (хемилюминесцентный тест с перекисью водорода) измеряет способность нейтрофилов продуцировать активные формы кислорода (АФК), такие как супероксидный анион и перекись водорода, которые необходимы для уничтожения патогенов. В тесте нейтрофилы стимулируют и добавляют субстраты, которые излучают свет в присутствии АФК. Интенсивность свечения измеряется с помощью люминометра и используется для оценки оксидативной активности нейтрофилов, что особенно важно при диагностике состояний, таких как хроническое гранулематозное заболевание.


