Общий тестостерон в крови
Информация об исследовании
Анализ определяет суммарную концентрацию тестостерона в сыворотке крови. Тестостерон — главный мужской половой гормон, который относится к группе андрогенов и вырабатывается у мужчин преимущественно в яичках, а у женщин в значительно меньших количествах в яичниках, надпочечниках и периферических тканях из предшественников андрогенов. У мужчин тестостерон отвечает за развитие половых органов и вторичных половых признаков в пубертате, поддержание сперматогенеза, либидо и эректильной функции, мышечной массы и силы, плотности костной ткани, образование эритроцитов и нормальное настроение. У женщин тестостерон вырабатывается в меньших количествах, однако его роль не менее важна: он поддерживает либидо, мышечную массу, плотность костей, когнитивные функции и служит субстратом для синтеза эстрогенов в периферических тканях. В крови тестостерон циркулирует в трёх формах: небольшая свободная фракция, основная часть, связанная с глобулином, связывающим половые гормоны (ГСПГ), и часть, связанная с альбумином; биологически активна только свободная фракция и часть, связанная с альбумином. Главное клиническое применение анализа состоит в диагностике гипогонадизма у мужчин, диагностике синдрома гиперандрогении у женщин, оценке нарушений полового развития у подростков и мониторинге заместительной терапии.
Синтез и транспорт
У мужчин основным источником тестостерона являются клетки Лейдига в яичках, продуцирующие около 95% гормона. Около 5% циркулирующего тестостерона имеет надпочечниковое происхождение. В норме этот вклад минимален, однако он приобретает критическое клиническое значение при гормонально-активных опухолях надпочечников и врожденной дисфункции коры надпочечников (ВДКН), где избыточный синтез андрогенов становится ведущим патологическим фактором.
Суточная продукция составляет 5–7 мг, при этом секреция имеет выраженный циркадианный ритм с максимумом в утренние часы и минимумом вечером.
У женщин тестостерон образуется в сопоставимых долях из трёх источников: яичники продуцируют около 25% гормона, надпочечники — ещё 25%, а оставшиеся 50% образуются путём периферической конверсии из предшественников (андростендиона и дегидроэпиандростерона) в жировой ткани, коже и других органах. Общая суточная продукция у женщин составляет 0,1–0,4 мг, что в 15–20 раз меньше, чем у мужчин.
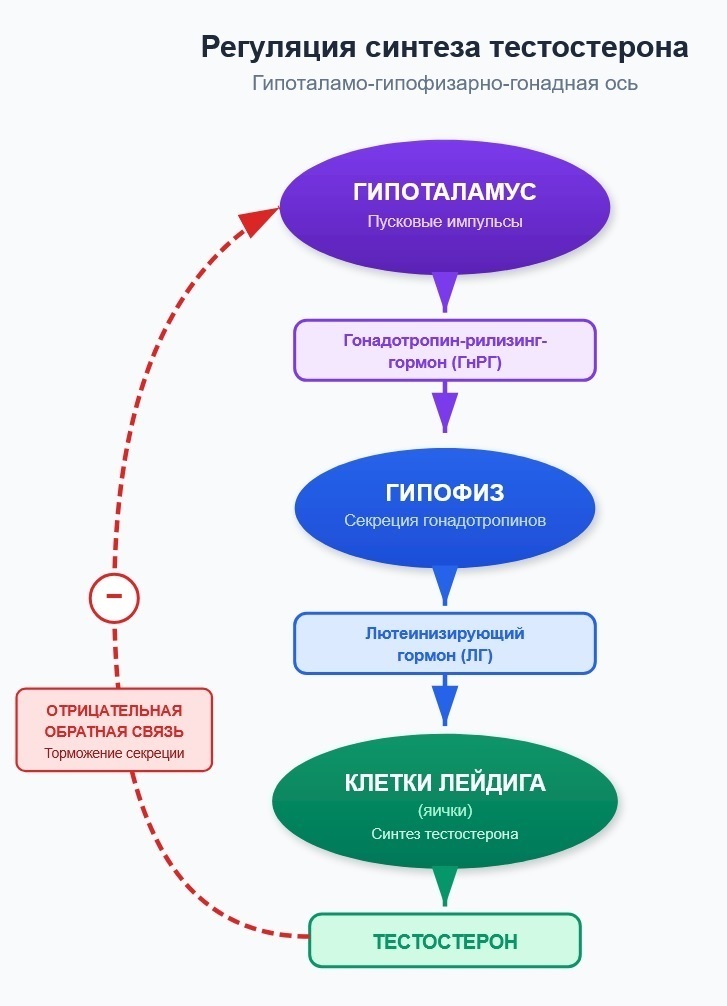
Регуляция синтеза осуществляется по оси гипоталамус-гипофиз-гонады. Гипоталамус вырабатывает гонадотропин-рилизинг-гормон, стимулирующий секрецию лютеинизирующего гормона (ЛГ) в гипофизе. ЛГ, в свою очередь, активирует продукцию тестостерона в гонадах. Тестостерон по механизму отрицательной обратной связи подавляет секрецию ЛГ и гонадотропин-рилизинг-гормона, замыкая регуляторный контур.
В крови тестостерон циркулирует в трёх формах. Около 2–3% представлено свободной фракцией, не связанной с белками и способной непосредственно проникать в клетки-мишени. Примерно 44% связано с глобулином, связывающим половые гормоны (ГСПГ), эта фракция метаболически неактивна. Оставшиеся 54% связаны с альбумином слабой связью, легко диссоциирующей в капиллярах тканей-мишеней. Сумма свободного тестостерона и фракции, связанной с альбумином, составляет биодоступный тестостерон, который и определяет клинические эффекты гормона.
Клиническое значение
Гипогонадизм у мужчин — главное показание к определению общего тестостерона. По уровню нарушения регуляции гипогонадизм делят на первичный (гипергонадотропный) и вторичный (гипогонадотропный). Первичный гипогонадизм развивается при непосредственном поражении яичек: синдроме Клайнфельтера (наиболее частая генетическая причина с кариотипом 47,XXY), крипторхизме, орхите вирусной этиологии (особенно после эпидемического паротита), травме или перекруте яичка, последствиях химиотерапии или лучевой терапии. Вторичный гипогонадизм обусловлен нарушением гипоталамо-гипофизарной регуляции и развивается при опухолях гипофиза и гипоталамической области, гиперпролактинемии, синдроме Каллмана с врождённым нарушением миграции гонадотропин-рилизинг-нейронов, гемохроматозе с накоплением железа в гипофизе. Отдельный механизм представляет функциональный гипогонадизм при ожирении, сахарном диабете 2 типа, хронических системных заболеваниях, длительном приёме глюкокортикоидов или опиоидных анальгетиков, который связан с подавлением гипоталамо-гипофизарной оси и обратим при устранении причины. Клинические проявления гипогонадизма включают снижение либидо и эректильную дисфункцию, уменьшение мышечной массы и силы, увеличение жировой ткани, гинекомастию, снижение плотности костей с риском переломов, депрессивные симптомы, утомляемость и анемию.
Возрастное снижение тестостерона у мужчин — отдельный физиологический процесс. После 30 лет уровень общего тестостерона снижается приблизительно на 1–2% ежегодно, что связано с уменьшением числа клеток Лейдига, снижением их чувствительности к лютеинизирующему гормону и возрастным повышением уровня ГСПГ. Симптоматический возрастной гипогонадизм требует подтверждения двумя независимыми измерениями утреннего уровня общего тестостерона при наличии клинических проявлений; согласно рекомендациям ISSAM диагностически значимым считается уровень общего тестостерона ниже 12 нмоль/л в сочетании с симптомами. Диапазон 8–12 нмоль/л составляет диагностическую «серую зону», в которой требуется определение свободного тестостерона и ГСПГ для уточнения биологически активной фракции гормона.
Синдром гиперандрогении у женщин — вторая основная задача анализа. Наиболее частой его причиной служит синдром поликистозных яичников (СПКЯ), затрагивающий около 6–15% женщин репродуктивного возраста. Согласно Роттердамским критериям, для диагноза необходимо наличие двух из трёх признаков: клиническая или биохимическая гиперандрогения, олиго- или ановуляция, поликистозная морфология яичников по данным УЗИ. Тестостерон при СПКЯ обычно умеренно повышен, иногда остаётся в пределах верхней границы нормы; для оценки биологически активной фракции рассчитывают индекс свободных андрогенов с учётом уровня ГСПГ. Неклассическая (поздняя) форма врождённой дисфункции коры надпочечников проявляется в пубертате или у молодых женщин гирсутизмом, акне, нарушениями менструального цикла; диагностически значимо повышение 17-гидроксипрогестерона. При значительном повышении тестостерона выше 5 нмоль/л и быстром нарастании симптомов вирилизации (огрубение голоса, клиторомегалия, мужской тип облысения) необходимо исключение андроген-секретирующей опухоли яичников или надпочечников. Гиперандрогения может также возникать при синдроме Кушинга, гипертекозе яичников и приёме андрогенных препаратов или анаболических стероидов.
Интерпретация результата общего тестостерона требует учёта концентрации ГСПГ, который определяет долю биологически активной фракции гормона. При высоком ГСПГ (гипертиреоз, цирроз печени, приём эстрогенов и противоэпилептических препаратов, ВИЧ-инфекция, пожилой возраст) большая часть тестостерона оказывается связанной и недоступной тканям, поэтому симптомы дефицита андрогенов могут присутствовать даже при нормальном общем уровне. Наоборот, при низком ГСПГ (ожирение, гипотиреоз, сахарный диабет 2 типа, нефротический синдром, приём глюкокортикоидов и андрогенов, акромегалия) свободная фракция увеличивается, и клинические эффекты могут проявляться при относительно невысоком общем уровне. В этих ситуациях клиническую картину уточняет определение свободного или биодоступного тестостерона. Однократное отклонение тестостерона от нормы недостаточно для постановки диагноза: согласно международным рекомендациям, требуется подтверждение повторным исследованием в тех же стандартизованных условиях.
Дифференциальная диагностика первичного и вторичного гипогонадизма у мужчин строится на сочетании уровня общего тестостерона с уровнями лютеинизирующего и фолликулостимулирующего гормонов гипофиза. При первичном поражении яичек снижение тестостерона сопровождается компенсаторным повышением ЛГ и ФСГ из-за ослабления отрицательной обратной связи; такая картина указывает на поражение на уровне гонад. При вторичном гипогонадизме нарушена гипоталамо-гипофизарная регуляция, и снижение тестостерона сопровождается нормальным или сниженным уровнем гонадотропинов; это требует визуализации гипофиза, исключения опухолей и оценки других тропных гормонов. Иммунохимические методы определения общего тестостерона недостаточно точны при низких концентрациях гормона, что особенно важно для женщин, детей и пациентов с тяжёлым гипогонадизмом; в этих ситуациях для уточнения предпочтительны методы жидкостной или газовой хроматографии с масс-спектрометрией.
Что влияет на результат анализа
Уровень тестостерона в крови подвержен значительным физиологическим колебаниям. Секреция имеет выраженный циркадианный ритм с максимумом в утренние часы и снижением к вечеру на 30–50%, поэтому забор крови проводят в период с 7 до 11 часов утра натощак. У женщин репродуктивного возраста анализ выполняют на 3–5 день менструального цикла. Накануне исследования следует исключить интенсивные физические нагрузки, эмоциональные перегрузки и приём алкоголя; курение прекращают за 30 минут до забора крови. На уровень тестостерона влияют многие лекарственные препараты: глюкокортикоиды, опиоидные анальгетики, антиандрогены (спиронолактон, финастерид, ципротерон), эстрогены и комбинированные оральные контрацептивы, противоэпилептические препараты, а также экзогенный тестостерон и анаболические стероиды. О всех принимаемых препаратах следует сообщить лечащему врачу. Острое системное заболевание, недавняя операция, тяжёлая травма и хронический стресс транзиторно снижают уровень тестостерона у обоих полов и не отражают истинного гонадного статуса.
Когда назначают анализ
Как подготовиться к анализу
Что означают результаты
Референсные значения
Приведённые интервалы валидированы для метода твердофазного хемилюминесцентного иммуноанализа (ХЛИА) на платформе Abbott Alinity i.
Референсные значения для мужчин
- Период новорождённости и раннего детства (4 дня — 6 месяцев): 0,30–10,36 нмоль/л.
Широкий диапазон значений в первые месяцы жизни обусловлен феноменом «мини-пубертата новорождённых». В этот период происходит транзиторная активация гипоталамо-гипофизарно-гонадной оси, унаследованная от внутриутробного периода. Уровень тестостерона у мальчиков может достигать значений, сопоставимых с нижней границей взрослой нормы, с пиком на 1–3 месяце жизни. К полугоду активность оси снижается, и концентрация гормона падает до минимальных значений. - Детский возраст (6 месяцев — 9 лет): < 1,24 нмоль/л.
Период физиологической супрессии гонадотропной оси, характеризующийся минимальными концентрациями тестостерона. Яички находятся в состоянии относительного покоя, и уровень гормона остаётся стабильно низким. Значения, превышающие верхнюю границу, требуют исключения преждевременного полового развития или андроген-секретирующих опухолей. - Препубертатный период (9–11 лет): < 0,81 нмоль/л.
У большинства мальчиков этого возраста сохраняется допубертатный статус с низким уровнем тестостерона. Однако у части детей уже начинается активация гонадной функции. При клинических признаках начала пубертата (увеличение объёма яичек более 4 мл) уровень тестостерона может превышать указанную границу, что является физиологичным и требует оценки в контексте стадии полового развития. - Ранний и средний пубертат (11–14 лет): < 15,41 нмоль/л.
Период активного полового созревания с выраженной индивидуальной вариабельностью как по срокам начала, так и по темпам прогрессирования. У мальчиков в начале пубертата (стадия Таннера II) уровень тестостерона составляет 0,5–3,5 нмоль/л, к середине пубертата (стадия III) достигает 2,0–15,0 нмоль/л. Отсутствие повышения тестостерона к 13–14 годам при наличии других признаков пубертата или, напротив, отсутствие признаков полового развития к 14 годам требует эндокринологического обследования. - Поздний пубертат (14–16 лет): 1,25–21,92 нмоль/л.
Продолжается активный рост концентрации тестостерона. Нижняя граница 1,25 нмоль/л отражает случаи конституциональной задержки полового развития, при которой мальчик в 14 лет может находиться ещё на ранних стадиях пубертата. Для подростков 15–16 лет с нормальным темпом развития (стадии Таннера IV–V) характерны значения 8,0–22,0 нмоль/л. - Завершение пубертата (16–18 лет): 5,13–27,53 нмоль/л.
Большинство юношей к 17–18 годам достигают взрослых значений тестостерона. Нижняя граница 5,13 нмоль/л допустима для 16-летних с продолжающимся созреванием, однако для 17–18-летних с завершённым развитием уровень ниже 8,0 нмоль/л требует внимания и при наличии клинических признаков гипогонадизма — дообследования. - Взрослые мужчины репродуктивного возраста (18–50 лет): 8,9–42,0 нмоль/л.
Референсный диапазон для мужчин в период максимальной гормональной активности. Пик секреции тестостерона приходится на 25–30 лет, после чего начинается постепенное физиологическое снижение. Значения в пределах указанного интервала обеспечивают нормальную сексуальную функцию, фертильность, мышечную массу, плотность костей и метаболическое здоровье.
Для клинической интерпретации принципиальное значение имеют диагностические пороги. Международное общество по изучению старения мужчин (ISSAM) рекомендует использовать нижний диагностический порог 12,0 нмоль/л. Уровень ниже этого значения при наличии характерных симптомов свидетельствует о гипогонадизме и требует дальнейшего обследования для установления его природы — первичной или вторичной.
Диапазон 8,0–12,0 нмоль/л представляет «серую зону», требующую оценки свободного тестостерона, уровня ГСПГ и клинической картины. Уровень выше 12,0 нмоль/л практически исключает дефицит андрогенов как причину имеющихся жалоб при нормальной концентрации ГСПГ.
Мужчины старшего возраста (старше 50 лет): 8,6–23,4 нмоль/л.
С возрастом происходит постепенное снижение уровня тестостерона приблизительно на 1–2% ежегодно. Это обусловлено уменьшением числа клеток Лейдига, снижением их чувствительности к лютеинизирующему гормону, а также возрастным повышением концентрации ГСПГ. К 70 годам средний уровень составляет около 70% от показателей молодого возраста.
Сужение референсного диапазона (снижение верхней границы с 42,0 до 23,4 нмоль/л) отражает физиологическую инволюцию гонадной функции. Тем не менее нижняя граница остаётся практически неизменной (8,6 нмоль/л), и симптоматический гипогонадизм диагностируется по тем же критериям, что и у молодых мужчин: уровень ниже 12,0 нмоль/л (рекомендация ISSAM) при наличии клинических проявлений.
Референсные значения для женщин
У женщин тестостерон вырабатывается яичниками, надпочечниками и путём периферической конверсии из предшественников. Общая продукция в 15–20 раз ниже, чем у мужчин, однако физиологическая роль андрогенов включает поддержание либидо, мышечной массы, плотности костей и когнитивных функций.
- Детский возраст (4 дня — 9 лет): < 2,15 нмоль/л.
В первые месяцы жизни у девочек также наблюдается транзиторная активация гонадной оси, хотя и менее выраженная, чем у мальчиков. К концу первого года жизни уровень тестостерона снижается до минимальных значений и остаётся низким на протяжении всего детства. Превышение верхней границы требует исключения врождённой гиперплазии коры надпочечников, преждевременного адренархе или андроген-секретирующих опухолей. - Препубертатный и ранний пубертатный период (9–13 лет): < 0,98 нмоль/л.
Период адренархе, когда начинается созревание сетчатой зоны коры надпочечников с увеличением продукции надпочечниковых андрогенов. Уровень тестостерона остаётся низким, однако постепенно начинает повышаться. Значения выше указанной границы при наличии признаков преждевременного полового развития (телархе, пубархе до 8 лет) требуют обследования. - Средний пубертат (13–15 лет): 0,36–1,54 нмоль/л.
Активное половое созревание с установлением овуляторных циклов. Яичники становятся значимым источником андрогенов. Появление нижней границы референсного интервала отражает необходимость минимального уровня андрогенов для нормального развития. - Поздний пубертат (15–18 лет): 0,49–1,70 нмоль/л.
Завершение полового созревания и достижение взрослого типа гормональной регуляции. Уровень тестостерона стабилизируется в пределах, характерных для женщин репродуктивного возраста. Значения выше верхней границы требуют исключения синдрома поликистозных яичников и других причин гиперандрогении. - Женщины репродуктивного возраста (18–50 лет): 0,52–1,72 нмоль/л.
Референсный диапазон для женщин в период максимальной репродуктивной активности. Уровень подвержен незначительным колебаниям в зависимости от фазы менструального цикла с небольшим пиком в периовуляторном периоде.
Повышение выше верхней границы требует углублённого обследования. Наиболее частой причиной умеренной гиперандрогении является синдром поликистозных яичников. Уровень выше 3,5–5,0 нмоль/л, особенно при быстром нарастании симптомов вирилизации (гирсутизм, акне, алопеция, огрубение голоса, клиторомегалия), подозрителен на андроген-секретирующую опухоль яичников или надпочечников и требует срочной визуализации.
Снижение ниже нижней границы может наблюдаться при гипопитуитаризме, надпочечниковой недостаточности, приёме комбинированных оральных контрацептивов. Клиническое значение низкого тестостерона у женщин изучено меньше, чем у мужчин, однако выраженный дефицит может проявляться снижением либидо, утомляемостью, депрессивными симптомами.
Беременность: до 3–4-кратного превышения значений небеременных
Во время беременности происходит физиологическое повышение уровня тестостерона, которое может достигать 5,0–7,0 нмоль/л к третьему триместру. Это обусловлено стимулирующим влиянием хорионического гонадотропина на текальные клетки яичников, а также продукцией андрогенов фетоплацентарным комплексом. Параллельно значительно возрастает концентрация ГСПГ, что ограничивает биологическую активность циркулирующего тестостерона и защищает плод от вирилизации.
Женщины в постменопаузе (старше 50 лет): 0,46–1,18 нмоль/л.
После прекращения функции яичников концентрация тестостерона снижается. Основным источником становятся надпочечники и периферическая конверсия из предшественников. Сужение референсного диапазона (снижение верхней границы с 1,72 до 1,18 нмоль/л) отражает возрастное уменьшение продукции андрогенов.
Выраженный дефицит тестостерона в постменопаузе может усугублять снижение либидо, утомляемость, потерю мышечной массы и плотности костей. Рутинное определение тестостерона у женщин в постменопаузе при отсутствии специфических жалоб не рекомендуется.
Причины отклонений уровня тестостерона
Снижение тестостерона у мужчин
Снижение тестостерона – гипогонадизм у мужчин подразделяется на первичный (гипергонадотропный) и вторичный (гипогонадотропный) в зависимости от уровня поражения.
Первичный гипогонадизм развивается при непосредственном поражении яичек.
- Синдром Клайнфельтера (кариотип 47,XXY) является наиболее частой генетической причиной, встречающейся у 1 из 600 новорождённых мальчиков. Характерны высокий рост, евнухоидные пропорции, гинекомастия, маленькие плотные яички, бесплодие.
- Крипторхизм (неопущение яичек) при несвоевременной коррекции приводит к необратимому повреждению герминативного эпителия и клеток Лейдига вследствие воздействия повышенной температуры брюшной полости. Двусторонний крипторхизм без лечения практически всегда сопровождается гипогонадизмом.
- Орхит, особенно вирусной этиологии (эпидемический паротит), может вызывать атрофию яичек с последующим снижением продукции тестостерона. Риск развития гипогонадизма составляет 30–50% при двустороннем поражении.
- Травмы и перекрут яичка приводят к ишемическому повреждению ткани. Варикоцеле вызывает нарушение терморегуляции и микроциркуляции, что негативно влияет как на сперматогенез, так и на стероидогенез.
- Химиотерапия и лучевая терапия оказывают дозозависимое повреждающее действие на гонады. Алкилирующие агенты (циклофосфамид, хлорамбуцил) наиболее гонадотоксичны. Облучение области таза повреждает герминативный эпителий уже при дозах 1–2 Гр; функция клеток Лейдига у взрослых нарушается при дозах свыше 20–30 Гр, у препубертатных мальчиков — при дозах около 12 Гр.
- Возрастной гипогонадизм (андрогенный дефицит пожилых мужчин) развивается вследствие постепенного снижения функции клеток Лейдига, уменьшения их численности и ослабления чувствительности к ЛГ. К 70 годам около 30% мужчин имеют уровень тестостерона ниже нижней границы нормы молодых.
Вторичный гипогонадизм обусловлен нарушением гипоталамо-гипофизарной регуляции.
- Опухоли гипоталамо-гипофизарной области (аденомы гипофиза, краниофарингиомы, герминомы) вызывают компрессию или деструкцию гонадотрофов. Пролактинома заслуживает особого внимания: гиперпролактинемия подавляет секрецию гонадотропин-рилизинг-гормона, приводя к гипогонадизму даже при небольших размерах опухоли.
- Синдром Каллмана представляет собой врождённое нарушение миграции гонадотропин-рилизинг-гормон-продуцирующих нейронов, сочетающееся с аносмией или гипосмией. Характерны задержка пубертата, евнухоидные пропорции, крипторхизм.
- Гемохроматоз приводит к отложению железа в гипофизе с избирательным повреждением гонадотрофов. Гипогонадизм нередко является первым эндокринным проявлением заболевания и может предшествовать развитию цирроза печени и сахарного диабета.
- Ожирение ассоциировано со снижением тестостерона по нескольким механизмам: подавление секреции гонадотропинов избытком эстрогенов (образующихся путём ароматизации андрогенов в жировой ткани), снижение уровня ГСПГ, прямое ингибирующее действие лептина и провоспалительных цитокинов на гипоталамо-гипофизарную ось. У мужчин с индексом массы тела более 40 кг/м² распространённость гипогонадизма достигает 50%.
- Сахарный диабет 2 типа сопровождается гипогонадизмом у 30–50% пациентов. Механизмы включают инсулинорезистентность, висцеральное ожирение, хроническое воспаление, прямое токсическое действие гипергликемии на клетки Лейдига.
- Хронические системные заболевания (хроническая болезнь почек, цирроз печени, ХОБЛ, ВИЧ-инфекция, ревматоидный артрит) вызывают функциональный гипогонадизм вследствие подавления гипоталамо-гипофизарной оси провоспалительными цитокинами, нарушения метаболизма стероидов, кахексии.
Ятрогенные причины занимают значительное место в структуре гипогонадизма.
- Глюкокортикоиды подавляют секрецию гонадотропинов дозозависимо. Даже низкие дозы преднизолона (5–7,5 мг/сут) при длительном приёме могут снижать уровень тестостерона.
- Опиоидные анальгетики вызывают гипогонадизм у 50–90% пациентов, получающих хроническую терапию через подавление секреции гонадотропин-рилизинг-гормона на уровне гипоталамуса. Эффект дозозависим и обратим при отмене препарата.
- Анаболические стероиды и экзогенный тестостерон по механизму отрицательной обратной связи подавляют эндогенную продукцию гормона и могут вызывать длительную супрессию гипоталамо-гипофизарно-гонадной оси, сохраняющуюся месяцы и годы после прекращения приёма.
- Антиандрогенные препараты (спиронолактон, финастерид, ципротерона ацетат) снижают эффективный уровень андрогенов либо за счёт блокады рецепторов, либо путём ингибирования 5α-редуктазы.
Повышение тестостерона у мужчин
Изолированное повышение тестостерона у мужчин без экзогенного введения встречается относительно редко и требует исключения серьёзной патологии.
- Андроген-секретирующие опухоли яичек (лейдигомы) продуцируют тестостерон автономно, независимо от регуляции ЛГ. Характерны уровни тестостерона выше 40–50 нмоль/л при подавленных гонадотропинах. Опухоль может быть непальпируемой и выявляться только при УЗИ.
- Андроген-секретирующие опухоли надпочечников чаще продуцируют предшественники (ДГЭА, андростендион), однако могут вызывать значительное повышение тестостерона. Сочетание гиперандрогении с гиперкортицизмом характерно для карциномы коры надпочечников.
- Врождённая гиперплазия коры надпочечников (ВДКН) у мужчин с неклассической формой может манифестировать во взрослом возрасте повышением тестостерона, бесплодием, образованием опухолеподобных узлов в яичках (testicular adrenal rest tumors).
- Резистентность к андрогенам (частичная форма) сопровождается компенсаторным повышением тестостерона при сниженной чувствительности рецепторов.
- Приём экзогенного тестостерона или анаболических стероидов является наиболее частой причиной повышенного уровня у молодых мужчин. При использовании инъекционных форм характерны значительные колебания уровня гормона.
Снижение тестостерона у женщин
Изолированное снижение тестостерона у женщин имеет меньшее клиническое значение, чем у мужчин, однако выраженный дефицит может сопровождаться характерной симптоматикой.
- Гипопитуитаризм любой этиологии (опухоли, облучение, синдром Шихана, лимфоцитарный гипофизит) приводит к снижению как гонадотропинов, так и АКТГ, что уменьшает продукцию андрогенов яичниками и надпочечниками.
- Первичная надпочечниковая недостаточность (болезнь Аддисона) сопровождается дефицитом надпочечниковых андрогенов. Уровень тестостерона и ДГЭА-сульфата снижен.
- Преждевременная недостаточность яичников (ранняя менопауза до 40 лет) вызывает снижение овариальной продукции андрогенов.
- Двусторонняя овариэктомия приводит к резкому падению уровня тестостерона на 50%, поскольку устраняется яичниковый источник.
- Приём комбинированных оральных контрацептивов значительно повышает уровень ГСПГ (в 2–4 раза), что снижает свободную фракцию тестостерона даже при нормальном общем уровне. Кроме того, этинилэстрадиол подавляет продукцию андрогенов яичниками.
- Гипотиреоз сопровождается снижением уровня тестостерона вследствие уменьшения продукции и изменения метаболизма андрогенов.
- Хронические заболевания, нервная анорексия, чрезмерные физические нагрузки (триада спортсменок) вызывают функциональный гипогонадизм с подавлением продукции андрогенов.
Повышение тестостерона у женщин
Гиперандрогения у женщин является распространённой эндокринной патологией и требует тщательной дифференциальной диагностики для выбора адекватной терапевтической тактики.
1. Функциональная гиперандрогения наиболее частая категория.
- Синдром поликистозных яичников (СПКЯ) является ведущей причиной гиперандрогении, затрагивая 6–15% женщин репродуктивного возраста. Диагностические критерии (Роттердам, 2003) включают наличие двух из трёх признаков: клиническая или биохимическая гиперандрогения, олиго- или ановуляция, поликистозная морфология яичников при УЗИ. Характерно умеренное повышение ЛГ при нормальном или сниженном ФСГ (соотношение ЛГ/ФСГ более 2–3).
- Гипертекоз яичников представляет собой тяжёлую форму овариальной гиперандрогении с наличием островков лютеинизированных текальных клеток в строме яичников. Уровень тестостерона выше, чем при типичном СПКЯ, выражена инсулинорезистентность, вирилизация более значительна.
- Идиопатический гирсутизм диагностируется при наличии избыточного роста волос при нормальном уровне андрогенов и регулярном овуляторном цикле. Причиной является повышенная активность 5α-редуктазы в коже или увеличенная чувствительность волосяных фолликулов к андрогенам.
2. Надпочечниковая гиперандрогения
Врождённая гиперплазия коры надпочечников (ВДКН) обусловлена генетическим дефектом ферментов стероидогенеза, чаще всего 21-гидроксилазы. Неклассическая (поздняя) форма манифестирует в пубертате или постпубертате симптомами гиперандрогении: гирсутизмом, акне, нарушениями цикла. Уровень тестостерона умеренно повышен, диагностически значимо повышение 17-гидроксипрогестерона (базального более 6 нмоль/л или стимулированного АКТГ более 30 нмоль/л).
Синдром Кушинга (эндогенный гиперкортицизм) сопровождается гиперандрогенией вследствие избыточной стимуляции надпочечников АКТГ или автономной продукции андрогенов опухолью. Характерны типичные кушингоидные черты: центральное ожирение, лунообразное лицо, стрии, артериальная гипертензия, нарушение толерантности к глюкозе.
3. Опухолевая гиперандрогения
Андроген-секретирующие опухоли яичников (арренобластома, опухоли из клеток Сертоли-Лейдига, липидоклеточные опухоли, гранулёзоклеточные опухоли) являются редкой, но клинически значимой причиной гиперандрогении. Характерны уровень тестостерона выше 5,0–7,0 нмоль/л (нередко более 10,0 нмоль/л), быстрое прогрессирование вирилизации (месяцы), отсутствие подавления тестостерона при назначении дексаметазона. Опухоль может быть небольшой и не определяться при стандартном УЗИ.
Андроген-секретирующие опухоли надпочечников (аденомы, карциномы) проявляются выраженной гиперандрогенией, часто в сочетании с гиперкортицизмом. Характерно значительное повышение ДГЭА-сульфата (более 15–20 мкмоль/л). Карцинома коры надпочечников отличается агрессивным течением и требует срочного хирургического лечения.
4. Ятрогенная гиперандрогения
Приём андрогенных препаратов (тестостерон, ДГЭА, анаболические стероиды) с целью улучшения спортивных результатов, повышения либидо или «омоложения» вызывает дозозависимое повышение уровня тестостерона.
При отсутствии жалоб рутинный скрининг не рекомендуется. При наличии симптомов или на фоне заместительной терапии — по назначению врача, обычно каждые 3–6 месяцев.
Секреция тестостерона подчиняется суточному ритму. Максимальные значения наблюдаются в 7–10 часов утра, к вечеру уровень может снижаться на 30–50%. Для стандартизации результатов кровь сдают в утренние часы.
Да, хронический стресс и недосыпание подавляют секрецию тестостерона. Острый стресс накануне исследования также может исказить результат.
Однократное отклонение требует повторного исследования через 2–4 недели. Только подтверждённое отклонение является основанием для дальнейшего обследования. Обязательно проконсультируйтесь с врачом.
Нормализация веса, регулярные силовые тренировки, полноценный сон, отказ от алкоголя и курения способствуют поддержанию оптимального уровня. Однако при истинном гипогонадизме этих мер недостаточно.
Стоимость исследования
биоматериала 240 ₽
биоматериала 240 ₽
